Conocer como se comportan los fertilizantes cuando se combinan entre sí, ademas de conocer perfectamente que fertilizantes pueden combinarse entre sí, es fundamental para eficiente uso de los fertilizantes.
Antes de comenzar, debemos de tener claro a que se refiere el termino «compatibilidad». Hoy día existen diversas fuentes de nutrientes vegetales y estas se comportan de una u otra manera cuando interactúan entre sí. Usualmente en fertirriego suelen prepararse soluciones nutritivas, estas soluciones tienen una concentración de los diversos nutrientes que la componen relativamente baja, con conductividad eléctrica relativamente baja , 2 dS/m en promedio. Y también se suelen usar soluciones nutritivas concentradas, es decir con conductividades eléctricas superiores a 10 dS/m, es en estas circunstancias es cuando la compatibilidad de los fertilizantes cobra importancia.
En fertirriego, en un sistema de riego, se suelen tener distintos tanques de solución concentrada, normalmente se usa uno para la fuente de calcio, otro para las fuentes de sulfato y uno más para la fuente de fosfato, además de tener uno para la inyección de ácidos. Cuando nos referimos al termino compatibilidad hablamos de fertilizantes que pueden mezclarse en altas concentraciones, (por altas concentraciones nos referímos a mas de 10 veces concentrado).
Algunos fertilizantes utilizados en la fertirrigación de cultivos pueden no ser compatibles entré si. Un ejemplo de incompatibilidad es la precipitación de sulfatos al combinarse con calcio. Conocer las compatibilidad entre los fertilizantes evita problemas de precipitación y disminución de la disponibilidad de los nutrientes por interacciones químicas. Otra incompatibilidad es la de los sulfatos con los fosfatos que también se precipitan. El hecho de que un nutriente se precipite significa que no estará en solución del suelo, la planta no podrá absorber al nutriente pesar de que este se encuentre en el suelo o sustrato.
Compatibilidad de fertilizantes para fertirrigación
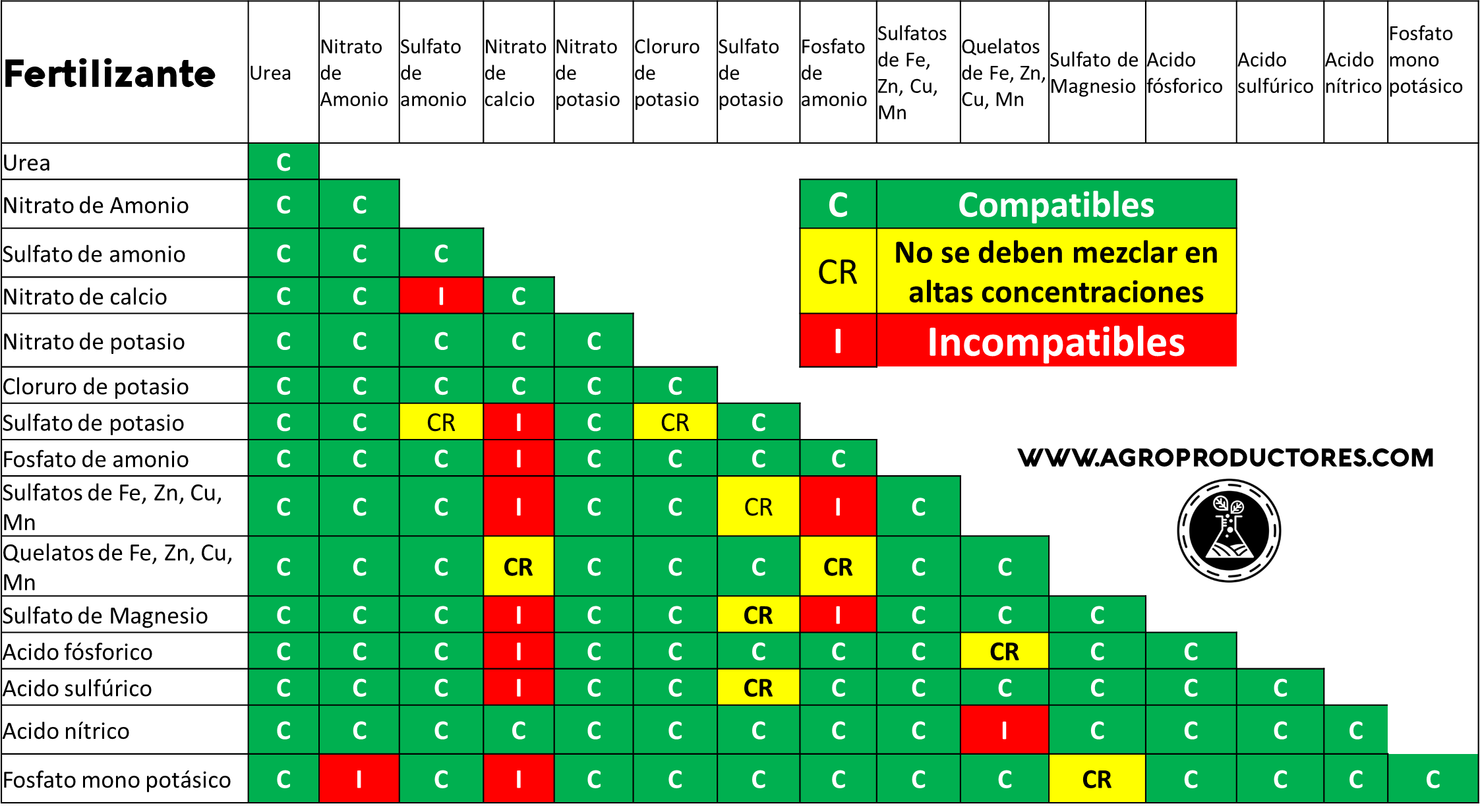
En la tabla de abajo se muestran las compatibilidades de diversos fertilizantes usados en el fertirriego.

En la tabla de abajo se añade la compatibilidad del fosfato mono potásico, que es una fuente de fósforo y potasio, un fertilizante utilizado ampliamente en la fertirrigación.

Consideraciones importantes al mezclar fertilizantes
Nitrato de amonio: Muy soluble, acidificante, elevada capacidad de salinización.
Nitrato de calcio: Completa incompatibilidad con sulfato de magnesio, nitrato de amonio y sulfato de potasio.
Fosfato tri cálcico: en aguas cálcicas y pH 6.5 existen precipitaciones, son más eficientes para estos casos los fosfatos mono amónicos, biamonicos o el ácido fosfórico concentrado.
Efectos antagónicos y sinérgicos de los elementos nutritivos en la solución del suelo. Por ejemplo, en suelos con elevado contenido de fosfatos y pH superiores a 7 no se debe aplicar sulfatos de hierro u oxidos de hierro como fuente de dicho elemento. Esto por que en estas condiciones estas fuentes se vuelven insolubles y por lo tanto no llegan a la solución del suelo. Para este tipo de suelo es recomendable utilizar hierro quelatado con un agente quelante de alta estabilidad, como lo es un EDDHA y HBED.
Nunca deben mezclarse fertilizantes que en su composición tengan hierro, fósforo y calcio, porque estos se vuelven insolubles. La compatibilidad entre fertilizantes que aportan estos nutrientes determina las fuentes a utilizar en la elaboración de la solución nutritiva.
Siempre será necesario realizar un análisis de agua para determinar la cantidad de calcio y magnesio que el agua aporta y adecuar las soluciones nutritivas a estas necesidades.
Los nutrientes conocidos como micronutrientes: Mg, Mn, Fe, Zn y el elemento secundario Ca, interactúan fuertemente con otros elementos presentes en el suelo, y pueden precipitarse o no estar disponibles para la planta debido a estas interacciones. Para solucionar este inconveniente en el mercado de los fertilizantes existe productos denominados quelatos que evitan este tipo de interacciones negativas y aseguran la disponibilidad del nutriente.
Los fertilizantes potásicos deben disolverse bien antes de ser aplicados.
Consideraciones de compatibilidad para micronutrientes quelatados
Los quelatos comerciales deben incluir en etiqueta un rango de estabilidad para la fracción quelatada, esta rango indica en que estabilidad el quelato mantiene su estabilidad, si el quelato es añadido a una solución que este fuera de su rango de estabilidad, este se romperá liberando al hierro que protege y perdiendo su utilidad.
Normalmente el rango de estabilidad de los quelatos usados en la agricultura como EDTA, EDDHSA, EDDHA, DTPA, va de 3 a 11, por lo tanto no se debe mezclar con ácidos en concentraciones que den como resultado un pH menor a 3. Considerando que las pruebas de estabilidad se realizan con agua destilada, es aconsejable mantener los quelatos EDTA en soluciones mayores a 5 de pH.
Los quelatos no se deben aplicar en el tanque de ácidos debido a que en condiciones de pH muy bajos los agentes quelantes se destruyen y liberan al metal, por lo que se pierde el beneficio de protección del nutriente. La resistencia particular de cada quelato al pH depende de su tipo.
Tanques de solución madre de fertilizantes
Para obtener el máximo beneficio del sistema de fertirriego es recomendable tener entre 4-6 tanques de solución madre, incluyendo un tanque exclusivo para ácidos. Cuando se usan quelatos para abastecer los micronutrientes, es muy recomendable tener un tanque extra exclusivo para los micronutrientes. Esto debido a que los quelatos suelen mezclarse en el tanque junto a la fuente de calcio. Los quelatos pierden estabilidad con altas concentraciones de calcio y puede presentarse perdida de quelato.
Para evitar problemas de acumulamiento de sales en las mangueras de riego se recomienda comenzar y terminar los riegos solo con agua. La compatibilidad de los fertilizantes suele mostrarse en la ficha u hoja técnica que acompaña al producto.
Para los fertilizantes nitrogenados se recomienda verificar que el contenido de biuret sea menor al 1%. Debido a que provoca fitotoxicidad en las plantas.